Linea guida
Diabete
Ultima revisione: 02/2021 Ultima modifica: 03/2024
Aggiornamento 03/2024
- Nuove raccomandazioni sulla terapia antidiabetica di combinazione (escalazione terapeutica) (-> cap. 3.3)
- La sezione sugli antidiabetici orali è stata completamente rivista e aggiornata (-> cap. 3.3.1)
- La sezione sulla terapia insulinica è stata completamente rivista e aggiornata (-> cap. 3.3.2).
1.Classificazione (1)
Diabete di tipo 1
- Distruzione immunologicamente mediata delle cellule beta che porta a una carenza assoluta di insulina
- Il LADA (Latent Autoimmune Diabetes of the Adults) corrisponde al diabete di tipo 1 a insorgenza tardiva.
Diabete di tipo 2
- 90 % di tutti i diabetici adulti
- Resistenza all’insulina con carenza relativa di insulina; nel corso della malattia, l'insulina è necessaria a causa della deplezione delle cellule basali (il 5 %/anno dei diabetici di tipo 2 richiede una terapia insulinica).
MODY (Maturity Onset Diabetes of the Young)*
Ricordiamo nel caso di
- Pazienti giovani (< 30 anni)
- Storia familiare positiva per il diabete
- Mancanza di obesità
* MODY: disturbi genetici della secrezione di insulina. Poiché coinvolge mutazioni genetiche, il MODY si distingue nei pazienti giovani di età inferiore ai 30 anni, con storia familiare positiva per il diabete, che non rientrano nel gruppo del diabete di tipo 1 o 2 (assenza di autoanticorpi, assenza di obesità). La distinzione è importante perché alcuni di questi pazienti rispondono molto bene alle sulfoniluree.
Diabete gestazionale
- Il 30–60 % delle donne svilupperà il diabete di tipo 2 più tardi nella vita.
Altri tipi specifici di diabete
- Farmaci: glucocorticoidi, neurolettici, interferone alfa, ecc.
- Endrocrinopatie: malattia di Cushing, feocromocitoma, acromegalia.
2. Diagnostica
Anamnesi/esame fisico
Anamnesi familiare
- Diabete, sovrappeso, ipertensione, infarto, ictus, malattia renale.
Esame fisico
- Altezza, peso, sistema cardiovascolare, pressione sanguina, arterie periferiche, esame dei piedi.
Laboratorio
- Glucosio plasmatico, HbA1c, creatinina, potassio, sodio, ASAT, ALAT, stato delle urine per microalbinuria, TSH nel diabete di tipo 1, stato lipidico se necessario.
Criteri diagnostici (1)
Diabete mellito
- L‘HbA1c ≥ 6,5 % è diagnostica
- In caso di glucosio plasmatico occasionale: ≥ 11,1 mmol/l e sintomi classici (poliuria, polidipsia, perdita di peso) e glucosio plasmatico a digiuno: ≥ 7,0 mmol/l l’HbA1c deve essere misurato (oppure controllare i risultati ogni 3 mesi).
Screening del diabete
- Nei pazienti asintomatici si racommanda lo screening di routine mediante glucosio plasmatico a digiuno o dell’HbA1c (metodo standardizzato e validato secondo DCCT o IFFC).
Il TOTG viene eseguito solo in gravidanza - La diagnosi deve essere confermata da una seconda misurazione in un altro giorno. Se l’HbA1c è tra 5,7 e 6,5 %, si raccomanda di utilizzare uno degli altri metodi di misurazione per la seconda misurazione.
Cave: assicurarsi che il glucosio plasmatico sia misurato correttamente! L’HbA1c può essere utilizzato per lo screening solo se non sono presenti i seguenti fattori: emoglobinopatia, aumento dell’ec-turnover (come anemia emolitica, trasfusioni di sangue, emolisi subclinica nell HIV), grave insufficienza epatica o renale, diabete gestazionale, diabete di tipo 1 o diabete associato alla CF, assunzione di dosi elevate di vitamina C ed E, età superiore ai 70 anni.
Categorie a maggior rischio di sviluppare il diabete (pre-diabete)
- IFG (impaired fasting glucose): glucosio plasmatico 5,6–6,9 mmol/l, HbA1c: ≥ 5,7–6,4 %.
Nota
„Pre-diabete“ (IFG, HbA1c: 6,0–6,4 %) spesso progredisce verso il diabete (4). A questi pazienti dovrebbe essere raccomandato un adeguamento dello stile di vita (49); nei casi singoli, la metformina.
Maturity Onset Diabetes of the Young (MODY)
- Tipicamente pazienti giovani (< 30 anni) e svelti, spesso con AF positiva per il diabete.
- Nel sospetto di dabete di tipo 1, determinare innanzitutto gli anticorpi –> anti-GAD e anti-IA2 e il C-peptide. In assenza di anticorpi e di C-peptide > 500 pmol/l e obesità assente, considerare il MODY. Il chiarimento genetico (ad es. a Exeter nel Regno Unito o a Ginevra) non porta quasi alcun beneficio aggiuntivo poiché non cambia nulla nella terapia; di solito i costi (almeno CHF 1’000.–) non sono coperti dalle assicurazioni malattie.
Screening
Ogni 3 anni per tutte le persone di età superiore ai 40 anni (6, 8). In caso di rischio aumentato, prima e a intervalli più brevi (ogni 1–3 anni). I seguenti criteri giustificano un aumento del rischio (–> vedi anche mediX LG Check-up)
- Anamnesi familiare positiva
- Stato di diabete gestazionale o peso del bambino alla nascita > 4’100 g
- IFG/o HbA1c 6,0–6,4 % nell‘anamnesi
- Nuovo: in tutti gli adulti in sovrappeso o obesi di età compresa tra 35 e 70 anni (ogni 3 anni) –> vedi anche US Preventive Services Task Force
- Ipertensione arteriosa
- Dislipidemia
- Sindrome dell'ovaio policistico.
3. Terapia
3.1. Obiettivi terapeutici (3, 6, 7–10, 42)
- Stabilire insieme al paziente obiettivi terapeutici personalizzati per lo stile di vita (cambiamenti), il metabolismo del glucosio, lo stato lipidico, il peso corporeo, la pressione arteriosa. Occorre tenere conto dell’età, di altre malattie, della situazione sociale, della qualità della vita ecc. (vedi tabella 1)
- Obiettivo HbA1c
- 6,5–7,0 % nei pazienti giovani (fino ai 60 anni)
- Nei pazienti anziani (> 80 J.), multimorbidi o con una bassa aspettativa di vita, può essere appropriata un’HbA1c di 8,0–9 %. L’ipoglicemia deve essere evitata, soprattutto nei pazienti con aterosclerosi e nei pazienti anziani.
- Regola generale: i pazienti più giovani con diabete di tipo 2 possono beneficiare di un controllo glicemico più stretto (HbA1c < 7 %).
Tabella 1: obiettivi della terapia nel diabete di tipo 1 e di tipo 2
|
|
Diabete del tipo 1 |
Diabete del tipo 2 |
|
Pressione arteriosa |
< 140/90 mmHg* |
< 140/90 mmHg* |
|
HbA1c** |
Individuale 6,5–7 % dovrebbe essere l’obiettivo nei pazienti giovani |
Individuale 6,5–8,5 %
|
|
Glucosio a digiuno** |
< 7 mmol/l (plasma) |
< 7 mmol/l (plasma) |
|
Glucosio postprandiale** |
< 10 mmol/l |
Seconda dell‘HbA1c definita, ma di solito < 10 mmol/l |
|
Colesterolo LDL |
Come nel diabete di tipo 2 |
In tutti > 40 anni fino a 75 anni**** · LDL < 1.8 mmol/l*** · LDL < 1,4 mmol/l nei pazienti ad alto rischio Pazienti < 40 anni: solo in caso di rischio cardiovascolare |
|
Attività fisica |
Come nel diabete di tipo 2 |
30–60 min ogni giorno 150 min/settimana 2 x allenamenti di forza-/si resistenza |
* Nei diabetici < 65 anni si raccomanda una pressione < 130/80 mmHg se la terapia è tollerata.
** I valori si riferiscono alla misurazione nel plasma sanguino. Tuttavia, le misurazioni capillari e plasmatiche differiscono solo in minima parte, per cui è possibile effettuare una misurazione capillare. Solo nel caso di diabete gestazionale deve essere il plasma, poiché in questo caso un aumento minimo può già portare alla diagnosi di diabete gestazionale. Il controllo della glicemia non è assolutamente necessario nello studio. La determinazione dell’HbA1c è sufficiente per il controllo di routine.
*** Una dose fissa di statine („fire and forget“) dovrebbe essere scelta solo per i pazienti per i quali non è possibile una strategia treat-to-target.
**** Nei pazienti di età superiore ai 75 anni non si raccomanda iniziare una statina come profilassi primaria alla prima diagnosi di diabete. E ancora oggetto di discussione se si dovrebbe interrompere la terapia a questa età per la profilassi primaria. Per la terapia di riduzione dei lipidi vedi anche mediX GL Iperlipidemia.
Automisurazione della glicemia
- Non è stato dimostrato un beneficio di una regolare automisurazione giornaliera della glicemia nei diabetici di tipo 2 senza terapia insulinica (3, 20). Non si raccomanda di misurare la glicemia quotidianamente nel diabete di tipo 2 senza insulina, ma di utilizzare l’HbA1c come guida. Tuttavia, alcune misurazioni possono avere senso dopo aver consultato il medico (ad es. un profilo giornaliero di 4 punti alla settimana, cioè prima di colazione, pranzo, cena e riposo a letto)
- Tuttavia, l’automisurazione della glicemia è necessaria per i diabetici di tipo 2 in determinate situazioni, ad esempio se la situazione metabolica è instabile con frequenti ipoglicemie, se la dieta è cambiata di modo considerevole (ad es. diarrea) o prima di un viaggio in auto (vedi Cap. 3.5.)
- Per i diabetici di tipo 1, la misurazione dovrebbe essere effettuata prima di mangiare, fare esercizio fisico, guidare o svolgere altre attività potenzialmente pericolose, dopo il trattamento dell’ipoglicemia e prima di andare a letto
- Per i diabetici di tipo 1, un CGMS (Continuous Glucose Monitoring Systems, ad es. freestyle libre o Dexcom) è un grande sollievo e dovrebbe essere offerto loro. Un freestyle libre può essere preso in considerazione anche per i diabetici di tipo 2 con un regime di bolo di base, poiché la misurazione capillare è faticosa per tutti i diabetici. Condizioni per il freestyle libre: almeno 4 iniezioni di insulina al giorno (cioè bolo di base); può essere prescritto solo da un diabetologo.
Scheda riassuntiva del diabete
L’obiettivo terapeutico viene stabilito insieme al paziente e inserito nel passaporto del diabete
|
1. Ottimo controllo (HbA1c: 6,5–7,0 %) |
Gravidanza, bambini, retinopatia grave, trapianti d‘organo, neuropatia dolorosa |
|
2. Buon controllo (HbA1c: 7,0–7,5 %) |
Obiettivo per la maggior parte dei diabetici |
|
3. Terapia sintomatica (HbA1c: ≤ 9,0 %) |
Pazienti molto anziani, polimorbilità |
Nota: il modello di scheda di controllo del diabete (versione Equam) è pubblicato separatamente.
3.2. Misure non farmacologiche
- Consulenza diabetologica e nutrizionale per tutti i pazienti
- Intervento sullo stile di vita: cambiamento dietetico a lungo termine, attività fisica regolare, perdita di peso relativamente modesta nei pazienti in sovrappeso/obesi (circa 5–10 %) sono più efficaci degli antidiabetici orali (6).
3.3. Terapia farmacologica
Note sulla strategia terapeutica
- Poiché i cambiamenti dello stile di vita da soli spesso non portano all’obiettivo, è possibile iniziare immediatamente una terapia farmacologica per abbassare la glicemia. Tuttavia, se i valori di HbA1c sono vicini al corridoio target, è opportuno provare prima solo misure non farmacologiche
- L’approccio terapeutico raccomandato dà la priorità alla metformina, agli inibitori del SGLT-2 e agli agonisti del GLP-1 (vedi anche l’algoritmo, tabella 2 e il testo sottostante).
Algoritmo: terapia ipoglicemizzante per il diabete di tipo 2
|
Definire l'obiettivo terapeutico individuale per la glicemia |
|
|
Terapia di base |
|
|
Farmacoterapia per abbassare la glicemia |
|
A seconda dell’HbA1c e di fattori della malattia et della persona
⇒ Per i pazienti con HbA1c < 8,5 % e a seconda della motivazione al cambiamento della dieta/all’attività fisica, cominciare con la monoterapia con metformina o una combinazione di due |
|
Monoterapia con metformina (1a scelta) |
|
|
Combinazione di due farmaci |
|
|
Se non si raggiunge l’obiettivo individuale per il HbA1c |
|
Tripla combinazione |
|
Metformina + SGLT-2 + GLP-1 è la combinazione preferita, attenzione all’approvazione dei costi
Se queste condizioni non sono soddisfatte
Nota: le sulfoniluree non sono più raccomandate officialmente dalla SSED; però possono essere utilizzate in casi eccezionali (ad es. intolleranza di altri antidiabetici orali) |
|
Se l'obiettivo individuale di HbA1c non viene raggiunto |
|
Terapia insulinica |
|
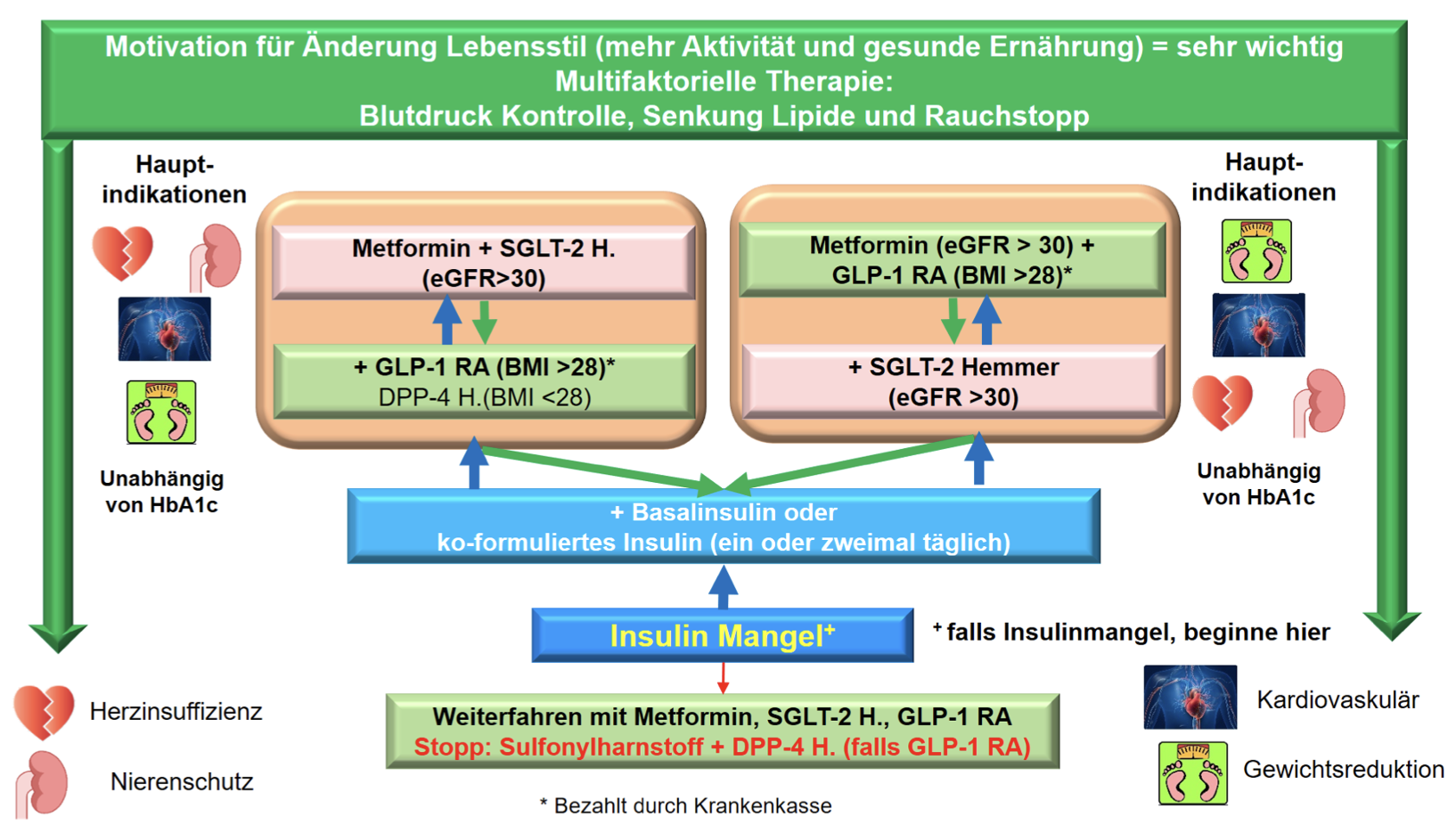
Terapia iniziale
Fase 1: Monoterapia
- Monoterapia con metformina
Gli inibitori SGLT-2 o gli analoghi del GLP-1 sono preferiti in caso di intolleranza o controindicazione alla metformina. Gli inibitori della DPP-4 sono utilizzati in caso di IMC
< 28 kg/m2 e controindicazione/intolleranza agli inibitori della SGLT-2 (frequenti infezioni fungine/infezioni del tratto urinario). Le sulfoniluree non sono più raccomandate dalla SSED a causa dell'esacerbazione della disfunzione delle cellule beta, dell'aumento di peso e del rischio di ipoglicemia (sono ancora prescritte nei paesi poveri di risorse [alta efficacia, basso costo]) - Nei pazienti con HbA1c elevata (≥ 8,5–9,0%), si raccomanda fin dall'inizio una combinazione di due farmaci e si raccomanda la terapia insulinica in presenza di segni di carenza insulinica (perdita di peso, cattive condizioni generali) (vedi tabella 2).
Fase 2: combinazione di due farmaci
Se gli obiettivi glicemici non vengono raggiunti con la fase 1 (dopo 3 a 6 mesi)
- Un secondo antidiabetico in aggiunta alla metformina. Sono da preferire gli analoghi del GLP-1 o gli inibitori del SGLT-2
- Un agonista GLP-1 è preferibile se la perdita di peso è una preoccupazione primaria et l’IMC è > 28 kg/m2 (utile nei pazienti con mancanza di sazietà/porzioni di pasti abbondanti)
- Un inibitore SGLT-2 è preferibile in caso di insufficienza cardiaca e renale
- Inibitori della DPP-4 in caso di IMC < 28 kg/m2 et effetti collaterali agli inibitori SGLT-2
- Alternativa insulina di base: più alta l‘HbA1c, più efficace deve essere la terapia. Se HbA1c
> 8,5 %, l’insulina è sempre una buona indicazione.
Fase 3: tripla combinazione
Se gli obiettivi glicemici non vengono raggiunti con la combinazione di due farmaci 2 (dopo 3 a 6 mesi)
- Iniziare la tripla terapia: è preferita una combinazione di metformina, inibitore del SGLT-2 e agonista del GLP-1. Per motivi di costo, l’assicurazione malattie richiede (ancora) una garanzia d’assunzione dei costi per la combinazione inibitori SGLT-2 e agonisti del GLP-1.
Giustificazione per l’aggiunta di un inibitore SGLT-2: insufficienza cronica renale o cardiaca (ad es. evidenza di TIG ridotto, microalbuminuria, EF ridotta).
Giustificazione per l’aggiunta di un agonista GLP-1: IMC > 28 kg/m2 - Se non sono soddisfatte le condizioni per una combinazione di agonista GLP-1 e inibitore SGLT-2, come alternativa a metformina e SGLT-2 si può amministrare un inibitore DPP-4, e come alternativa a metformina e GLP-1 si può usare un’insulina di base.
Fase 4: terapia insulinica
Se gli obiettivi glicemici non vengono raggiunti con la tripla combinazione (dopo 3 a 6 mesi)
Aggiungere o aumentare l’insulina! Nessun altro antidiabetico orale!
- Insulina di base (1 iniezione al giorno)
- Insulina coformulata = insulina mista = Ryzodeg (2 iniezioni al giorno)
- Insulina di base in bolo (4 iniezioni al giorno).
Il numero di iniezioni si definisce a seconda del livello del HbA1c, vuol dire il grado di deragliamento. L’obiettivo della diabetologia è evitare i boli di base. Se l’HbA1c aumenta (HbA1c > 8,5 %), considerare precocemente l’insulina di base, che spesso può stabilizzare il diabete per un periodo di tempo più lungo.
3.3.1. Antidiabetici orali (AO)/antidiabetici non insulinici
1. Metformina (Glucophage® e generici)
- Migliora la resistenza all’insulina, inibisce la gluconeogenesi epatica. L’antidiabetico orale con i migliori dati, neutro rispetto al peso, nessuna ipoglicemia
- Dosaggio: a causa degli effetti collaterali gastrointestinali (diarrea), introdurre gradualmente: 500 mg prima di cena e aumentare di 500 g ogni 4–5 giorni. Dose abituale di mantenimento e target: 2 x 1 g. Più di 2 g/giorno raramente porta a miglioramenti
- Controindicazioni: interrompere la metformina in caso di insufficienza renale con clearance della creatinina < 30 ml/min, se la clearance è di 30–45 ml/min, ridurre la dose (ad es. dimezzarla) e monitorare regolarmente la funzione renale (ogni 3 mesi) (30).
Nota: Informare il paziente di sospendere la metformina in caso di diarrea, riduzione dei liquidi, febbre, vomito - Avvertenza: la terapia a lungo termine con metformina può causare una carenza di vitamina B12 (a causa di assorbimento ridotto) (cave: interpretazione errata di neuropatia diabetica!). Possono essere utili controlli occasionali del livello di vitamina B12 (–> mediX LG Carenza di vitamina B12) (11, 31).
2. Inibitori SGLT-2
- Dapagliflozin (Forxiga®), canagliflozin (Invokana®, Vokanamet®), empagliflozin (Jardiance®, Jardiance Met®) e ertugliflozin (Steglatro®) inibiscono il riassorbimento del glucosio e ne aumentano l'escrezione nelle urine.
Dosaggi: dapagliflozin 5-10 mg, empagliflazone 10 mg (l'aumento della dose a 25 mg non porta alcun beneficio glicemico, ma aumenta gli effetti collaterali) - Nei diabetici con malattia cardiovascolare aterosclerotica, riduzione dell'insufficienza cardiaca, della mortalità cardiaca e complessiva. Effetti nefroprotettivi con prolungamento dell'aspettativa di vita in pazienti con insufficienza renale cronica (anche senza diabete) (48)
- Per i diabetici senza malattia cardiovascolare o renale
- Vantaggi: perdita di peso (ca. 5 kg), leggera riduzione della pressione arteriosa
(circa 4/2 mmHg) - Indicazione: adatto ai pazienti con malattia coronarica, in particolare con insufficienza cardiaca
- Insufficienza renale: al di sotto di un TIG di 15 ml/min, solo il canagliflozin ha un’indicazione, al di sopra di questo valore, possono essere utilizzati tutti gli inibitori
SGLT-2 - Effetti collaterali/svantaggi
- Infezioni del tratto urinario leggermente e rischio di infezione genitale (fungine) significativamente aumentato (circa il 10 %), soprattutto nelle donne
- Attenzione: con gli inibitori SGLT-2 e il diabete di tipo 1 è stata osservata chetoacidosi normoglicemica (–> somministrazione nel diabete di tipo 1 unicamente dal diabetologo). Nel diabete di tipo 2, sospendere in caso di diarrea, ridotta assunzione di liquidi, vomito, febbre.
- Vantaggi: perdita di peso (ca. 5 kg), leggera riduzione della pressione arteriosa
3. Agonisti del recettore GLP-1
|
Ingrediente |
Nome commerciale |
Intervallo di iniezione |
Disponibilità |
|
Semaglutide
|
Ozempic |
Settimanale s.c. |
Contingente, nessuna nuova prescrizione |
|
Rybelsus |
Giornaliero p.o. |
Senza restrizioni |
|
|
Dulaglutide |
Trulicity |
Settimanale s.c. |
Contingente, nessuna nuova prescrizione |
|
Tirzepatide |
Mounjaro |
Settimanale s.c. |
Presto in lista |
- Sono inoltre disponibili in combinazione con l'insulina: xultophy (liraglutide + insulina degludec [Tresiba®]), suliqua (lixisenatide + insulina glargine [Lantus®]). A seconda delle preferenze del paziente, l'insulina di base e l'agonista GLP-1 possono essere combinati in questi preparati
- Per l'obesità: Saxenda® (semaglutide per adolescenti fino a 18 anni) e Wegovy® (semiglutide per adulti)
Limitazioni per Wegovy®
Solo come coadiuvante di una dieta deficitaria da 500 kcal/die, di una consulenza nutrizionale concomitante e di un aumento dell'attività fisica documentato (ad es. pedometro) in pazienti motivati (senza precedente chirurgia bariatrica e senza chirurgia bariatrica programmata o imminente) per la gestione del peso in pazienti adulti con
IMC ≥ 35 kg/m2 o con
IMC ≥ 28 kg/m2 se sono presenti ulteriori comorbidità legate al peso (prediabete o diabete di tipo 2, ipertensione arteriosa, dislipidemia). -
A causa della domanda mondiale, gli agonisti GLP-1 (Ozempic e Trulicity) sono contingentati. Pertanto nessuna nuova prescrizione di agonisti s.c. del GLP-1, ma nuove impostazioni diRybelsus. Anche i pazienti con agonisti s.c. del GLP-1 per lungo tempo devono passare a Rybelsus. Dosaggi: Ozempic 0,25 mg = 3 mg Rybelsus 3 mg, Ozempic 0,5 mg = Rybelsus 7 mg e Ozempic 1 mg = 14 mg.Importante: per garantire l’assorbimento ottimale, assumere a digiuno almeno 30 minuti prima di qualsiasi altro farmaco, preferibilmente tra le 4 e le 6 del mattino quando si va in bagno.
- La tirzepatide (Mounjaro®) è un nuovo agonista del recettore GIP*-/GLP-1 di recente approvazione, caratterizzata in particolare da una riduzione significativamente maggiore del peso corporeo (51); inoltre, l’effetto ipoglicemico è più pronunciato nel confronto diretto con liraglutide (52).
A causa della mancanza di esperienza a lungo termine (e dei costi elevati), la tirzepatide si classifica inizialmente come farmaco di riserva. Il passaggio alla tirzepatide può essere considerato se non è possibile ottenere un controllo sufficiente della glicemia con la semaglutide/dulaglutide dosata.
* GIP= peptide insulinotropo glucosio-dipendente.
Nota: non associare gli agonisti del recettore GLP-1 e gli inibitori della DPP-4 (vedi sotto) perché hanno la stessa modalità d’azione!- Vantaggi: nessuna ipoglicemia, perdita di peso (talvolta significativa), cardioprottetivo e nefroprottetivo (44)
- Indicazione: particolarmente adatti ai pazienti obesi (IMC deve essere > 28 kg/m2) che soffrono per il loro peso e che hanno un rischio cardiovascolare elevato; consentito l’uso off-label per i diabetici di tipo 1 (se sono presenti problemi di peso), i costi sono parzialmente coperti dalle assicurazioni malattie dopo richiesta d’assunzione
- Insufficienza renale: gli studi dimostrano un uso sicuro fino alla dialisi, quindi senza problemi in caso di funzionalità renale ridotta (vedi schema sopra)
- Effetti collaterali/rischi: all’inizio, fino al 30 % di distrubi gastrointestinale (nausea), leggero aumento del rischio di calcoli biliari e altre malattie della cistifellea (47).
Avvertenza: i pazienti con retinopatia diabetica devono sottoporsi a una visita oculistica (e a successivi controlli) prima di iniziare la terapia, poiché la retinopatia diabetica può peggiorare con la terapia con agonisti GLP-1 (50).
Svantaggi: iniezione s.c.1 volta al giorno o 1 volta alla settimana, costi elevati.
4. Inibitori della DPP-4 (gliptine)
- Le gliptine inibiscono la dipeptidil peptidasi che, tra l’altro, inattiva l’incretina GLP-1 che viene secreta dopo l’assunzione di cibo e promuove la secretazione di insulina a seconda della glicemia. Nel caso di glicemia normale, non vi è alcuna stimolazione della secrezione di insulina.
Nota: non combinare gli inibitori della DPP-4 e gli agonisti del recettore del GLP-1, perché hanno la stessa modalità d’azione! - Farmaci: sitagliptine (Januvia®, Xelevia®), vildagliptine (Galvus®), linagliptine (Trajenta®), saxagliptine (Onglyza®), alogliptine (Vipidia®)
- Avantaggi: le gliptine possono essere assunte per via orale, non causano ipoglicemia e sono neutre dal punto di vista del peso. Possono essere utilizzati nell’insufficienza renale con aggiustamento della dose (non necessario con il linagliptine)
- Indicazione: è indicato per i pazienti con insufficienza renale, sovrappeso/obesità e nei quali è necessario evitare l’ipoglicemia
- Controindicazioni: epatopatia (con vildagliptine)
- Svantaggi: meno riduzione dell‘HbA1c rispetto alla metformina e le sulfoniluree. Più ricoveri in ospedale per insufficienza cardiaca con saxagliptine (34). Nessun effetto positivo sugli eventi cardiovascolari negli studi endpoint.
5. Sulfoniluree (SU)
- Stimolazione delle cellule beta. L'efficacia delle sulfoniluree generalmente diminuisce nel corso del trattamento. Sono quindi adatte alla monoterapia a lungo termine del diabete di tipo 2 solo in misura limitata, ma sono generalmente efficaci nei primi anni. Non sono più raccomandati nelle linee guida SSED 2023, ma sono ancora raccomandati nelle linee guida ADA 2024, in quanto sono una terapia efficace e poco costosa
- Gliclazide (Diamicron® e gliclazide generico): l'unica sulfonilurea da utilizzare. Gli studi di endpoint indicano effetti microvascolari favorevoli; può essere utilizzato anche nell'insufficienza renale fino a un TIG > 30 ml/min. Il rischio di ipoglicemia è basso
- Dosaggio: la dose iniziale è di 30–60 mg/d, 1 x al giorno come preparato a rilascio prolungato. La dose di mantenimento è di 1–3 compresse al giorno (4), assunte tutte in una volta (al mattino!). Dose massima giornaliera: 120 mg
- Effetti collaterali: soprattutto ipoglicemia e aumento di peso
- Non raccomandato
- Glibenclamide (Daonil®, Euglucon®, generici) (13)
- Glimepiride (Amaryl® e generici).
6. Glinidi
- Repaglinide (NovoNorm®). Modalità d'azione simile a quella delle sulfoniluree, ma inizio d'azione più rapido e durata d'azione più breve rispetto alle sulfoniluree
- Principio di assunzione: time to eat, time to treat
- Indicazione: nei pazienti con grave insufficienza renale grazie alla breve emivita; le glinidi devono essere prescritte dal diabetalogo solo in rari casi. Non sono più raccomandate nelle line guida della SSED del 2023
- Effetti collaterali: ipoclicemia
- Svantaggi: assumere ad ogni pasto, quindi la compliance è scarsa.
3.3.2.Terapia insulinica (3, 6, 8, 18,19)
Indicazione
- Aggiunta preferita a metformina, SGLT-2 e GLP-1
- Per i sintomi della carenza di insulina (perdita di peso, male condizione generale)
- HbA1c > 8,5 %: considerare l’inizio con insulina di base, > 9 % raccomandato
- Nelle donne in gravidanza (diabete preesistente o gestazionale).
Generalmente
- Prescrivere aghi corti (4–6 mm)
- Tutte le insuline sono vendite in confezioni da 5. Attenzione nella prescrizione: le penne preriempite (= Flextouch, Solostar) sono la regola rispetto alle fiale (Penfill) per i pazienti con penne di metallo.
Schema di terapia insulinica
Insuline di base
- In caso di diabete non sufficientemente controllato con la triplice terapia, aggiunta di un'insulina a lungo termine da iniettare una volta al giorno.
- Iniziare solitamente con Levemir®o Lantus® o Abasaglar®, in alternativa con le più costose insuline di base Tresiba® o Toujeo®
- Dosaggio: iniziare con 10 U (nei pazienti in sovrappeso anche di più), aumentare di 2 U ogni 2 giorni fino a una glicemia a digiuno < 8 mmol/l, idealmente 6–7 mmol/l.
Cave: non aumentare una dose di insulina di base pari a circa 1/3 del peso corporeo! In questi casi, bisogna aggiungere dell’insulina in bolo. Dosi elevate di insulina di base non sono in grado di abbassare la glicemia sufficientemente durante il giorno e portano a un ulteriore aumento di peso. - Nota
- L'insulina a lunghissima durata d'azione Tresiba® o Toujeo® può essere prescritta se si verifica un'iperglicemia mattutina nonostante il dosaggio di Levemir/Lantus/Abasaglar® o se la glicemia sale durante la notte o se il paziente necessita il sostegno a domicilio (l'iniezione di insulina prima del riposo a letto non è possibile), poiché Tresiba® e Toujeo® possono essere iniettate in qualsiasi momento (indipendentemente dall'ora grazie alla lunga emivita)
- Insulatard® è instabile e viene usato raramente al di fuori della gravidanza.
- Dosaggio: iniziare con 10 U (nei pazienti in sovrappeso anche di più), aumentare di 2 U ogni 2 giorni fino a una glicemia a digiuno < 8 mmol/l, idealmente 6–7 mmol/l.
Insuline miste = insuline coformulate
- Se il diabete non è ancora sufficientemente controllato con l'insulina di base dosata, è necessario aggiungere l'insulina in bolo, preferibilmente due volte al giorno come insulina coformulata
- Condizioni: una routine quotidiana molto regolare con pasti regolari e relativamente costanti. Le insuline miste sono ottime per i pazienti che consumano pasti molto regolari, in particolare per i pazienti anziani o residenti in case di cura. Non utilizzare nei pazienti più giovani a causa della mancanza di flessibilità!
- Dosaggio: prima dei 2 pasti prinicipali. Dose mattutina: copre la colazione e il pranzo, è regolata in base alla glicemia pre-cena. Dose serale: copre la cena e la notte, regolata in base alla glicemia a digiuno. Se il paziente consuma un pasto principalmente a mezzogiorno, le iniezioni possono essere somministrate a mezzogiorno e alla sera o al mattino e a mezzogiorno
- Rappresentante più importante = Ryzodeg®, contiene insulina aspartata (30 %) e insulina degludec (70 %). Esempio: 15 U Ryzodeg = 5 U insulina aspartata e 10 U insulina degludec. Raramente utilizzato è Humalog Mix (Humalog in combinazione con Insulatard (instabile)
- Dosaggio basato sulle dimensioni del pasto, ad esempio con 12 U prima di colazione e
10 U prima di cena, aumentare la dose a scatti di 4 U in base alla glilcemia misurata. - Per la determinazione della dose, viene creato un profilo glicemico giornaliero (misurazione della glicemia prima di colazione, pranzo e cena); appena viene individuata la dose appropriata, la frequenza di misurazione può essere ridotta (ad es. una volta ogni
10 giorni o solo l’HbA1c).
Terapia in bolo di base
- Consiste in insulina ad azione rapida ai pasti e insulina di base (4 iniezioni al giorno)
- Massima flessibilità, ma anche massima complessità
- La terapia esistente (metformina, agonista GLP-1, inibitore SGLT-2) viene lasciata inalterata
- A causa delle frequenti misurazioni della glicemia, viene sempre offerto un CGM (Freestyle libre o Dexcom, vedi sotto)
- Indicazione: nel diabete di tipo 2 se gli obiettivi terapeutici non possono essere raggiunti in altro modo
- Svantaggio: rischio maggiore di ipoglicemia.
⇒ Insuline in bolo: Insulin aspartat (Novorapid®, Fiasp®) Insulin lispro (Humalog®, Lyumjev®), Insulin glulisin (Apidra®)
- Durata d‘azione: 2–5 ore. Tutte le insuline hanno una curva di efficacia simile e sono ugualmente valide
- Fiasp® e Ljumjev® sono insuline ad azione ultrarapida con un inizio più rapido di circa
5 minuti rispetto a Novorapid® o Humalog ®. Ogni tanto vengono prescritte ai diabetici di tipo 1 per i quali è importante un intervallo di 15 minuti tra l’iniezione e il pasto.
⇒ Insuline di base
- Insuline di base di 2ª generazione = durata d’azione 24 ore, sono detemir (Levemir®), glargine (Lantus®, Abasaglar®)
- Sono tutti ugualmente validi, solo l'azienda è diversa (NovoNordisk vs. Sanofi).
- Insuline di base di 3ª generazione = durata d’azione ultralunga da circa 48 ore sono Tresiba® e Toujeo®
- Ultra-stabile, meno ipoglicemia.
|
Dosaggi di insulina |
|
Per il diabete di tipo 2 Per la prima prescrizione si raccomanda
Per il diabete di tipo 1 Rinvio al diabetologo (imparare a pesare i carboidrati, pompe per insulina) |
CGMS = continuous glucose measuring devices
- Sono offerti a tutti i pazienti con iniezioni di insulina 4 volte al giorno (regime di bolo di base) e sono rimborsati dalle assicurazioni malattie (è possibile l'autopagamento per iniezioni meno frequenti)
- Vantaggi
- L'utente non vede solo la glicemia attuale, ma anche una freccia di tendenza (in aumento, in diminuzione, stabile) che è utile per decidere le azioni da intraprendere (ad es. una glicemia elevata con freccia di tendenza in diminuzione può essere osservata e non corretta, una glicemia normale con freccia di tendenza in aumento può essere corretta)
- Nessuna misurazione capillare dolorosa, quest'ultima necessaria solo se si sospetta che il CGMS non sia corretto (ad es. una glicemia bassa segnalata senza sintomi di ipoglicemia).
- Svantaggi
- Timelag: il CGMS misura il glucosio a livello sottocutaneo e non capillare, quindi è in ritardo rispetto alla glicemia effettiva: nella vita di tutti i giorni, i vantaggi in termini di comfort e di freccia di tendenza superano questo svantaggio.
⇒ I seguenti CGMS sono disponibili
- Freestyle libre
- Freestyle libre 2: con funzione d’allarme per segnalare l’ipo- e l’iperglicemia
- Freestyle libre 3: come il 2, ma più piccolo e con trasmissione in tempo reale al telefonino (non è necessaria la scansione).
- Dexcom G7: stesse funzioni del Freestyle libre 3, forma e dimensione simili.
3.3.3. Terapia d’emergenza per l‘ipoglicemia
- Baqsimi® è un glucagone sotto forma di spray nasale che può essere somministrato a pazienti non coscienti. Si tratta di una somministrazione unica tramite pompa e sostituisce il precedente GLUCAGEN Novo Hypo-Kit, che doveva essere prima miscelato e poi somministrato per via intramuscolare (metodo più semplice)
- Procedura: vedi mediX Emergenze nello studio: ipoglicemia.
3.4. Controllo e trattamento delle malattie concomittanti
1. Abbassamento della pressione arteriosa
- Antipertensivi di prima scelta
- Inibitori ACE o bloccanti dell’AT-II; si può aggiungere diuretici a basso dosaggio (tiazidi, clortalidone) (24), seguiti da antagonisti del calcio, diuretici dell’ansa, alfa-bloccanti
- I beta-bloccanti devono essere utilizzati solo per indicazione cardiaca.
- Obiettivi per la pressione arteriosa
- Nei pazienti fino a 65 anni di età, mirare a un obiettivo di pressione ≤ 130/80 mmHg se la terapia antipertensiva è tollerata; ma non < 120 mmHg sistolica
- Nei pazienti di età superiore ai 65 anni, mirare a un obiettivo di pressione arteriosa
≤ 140/80 mmHg se la terapia è tollerata. Nei pazienti fragili e/o molto anziani, può essere necessario modificare gli obiettivi di pressione (≤ 150/90 mmHg).
Ulteriori informazioni sulla terapia antipertensiva –> mediX GL Ipertensione.
⇒ Nota: anche i diabetici senza pressione arteriosa elevata ma con microalbuminuria dovrebbero ricevere gli inibitori ACE (nefroprotezione).
2. Terapia ipoglicemizzante
- mediX raccomanda anche la terapia con statine a dosi fisse per i diabetici (strategia „fire and forget‟)
- Se in alternativa si sceglie la strategia „treat-to-target‟, si applicano le seguenti raccomandazioni
- Statine per tutti i diabetici in prevenzione primaria > 40–75 anni -> valore target LDL:
< 1,8 mmol/l - I diabetici di tipo 2 con danno agli organi terminali o almeno altri tre fattori di rischio cardiovasculare appartengono al gruppo ad alto rischio. Per loro si dovrebbe puntare a un valore target di LDL < 1,4 mmol/l. Questo vale anche per i diabetici di tipo 1 se si è già verificato un danno agli organi terminali (35).
- Statine per tutti i diabetici in prevenzione primaria > 40–75 anni -> valore target LDL:
⇒ Per ulteriori informazioni sul trattamento dell'iperlipidemia, sui valori target di LDL e sulla loro valutazione critica, si veda il documento mediX LG Iperlipidemia.
3. Aspirina (ASA)
- Non è più raccomandata la somministrazione come preventiva primaria (3, 22, 23, 46)
- L’ASA è raccomandata dalla SSED (3) solo per la prevenzione secondaria nelle malattie cardiovascolari conclamate.
mediX non raccomanda la somministrazione generale di aspirina nei diabetici. L’ASA può essere considerato nei pazienti ad alto rischio e dopo una valutazione clinica.
Controlli per ridurre le complicanze
1. Retinopatia diabetica
- Diabete di tipo 1: controllo oculistico 1–2 volte all’anno (la prima volta al più tardi dopo
5 anni) - Diabete di tipo 2: la prima volta alla diagnosi, in assenza di retinopatia ogni due anni, in presenza di retinopatia almeno una volta all’anno o su indicazione dell’oculista
- Per entrambe le forme: controllo immediato se l’acuità visiva si deteriora (in caso di forti fluttuazioni della glicemia, si tratta in genere di disturbi temporanei dell’accomadazione: effetto osmotico. Non regolare gli occhiali!)
- Mirare un buon controllo della pressione e della glicemia.
⇒ Template Controlli oftalmologici.
2. Nefropatia diabetica (3, 25)
- La microalbuminuria è considerata il primo segno di nefropatia
- Procedura: rapporto albumina-creatinina di un’urina spontanea nello studio: la microalbuminuria è presente a > 30 mg/g in 2 test su 3 in 4–6 mesi.
Nota: falso aumento dell‘escrezione di albuminuria in caso di attività fisica, infezioni, febbre, insufficienza cardiaca, iperglicemia marcata e prolungata, mestruazioni, ipertensione non controllata.
- Procedura: rapporto albumina-creatinina di un’urina spontanea nello studio: la microalbuminuria è presente a > 30 mg/g in 2 test su 3 in 4–6 mesi.
- Tutti i pazienti con microalbuminuria dovrebbero assumere un inibitore ACE o un bloccante AT-II
- Considerare gli inibitori del SGLT-2
- Mirare a un buon controllo del diabete e della pressione arteriosa
- Analisi delle urine: mediX non raccomanda l’analisi delle urine di routine per le IVU nei pazienti asintomatici. Un’IVU asintomatica non deve essere trattata nemmeno nel diabete.
Screening della microalbuminuria
- Diabete di tipo 1: annualmente (dopo 5 anni al più tardi)
- Diabete di tipo 2: annualmente (la prima volta alla diagnosi)
Nota: nel caso di microalbuminuria conosciuta, controllo annuale della proteinuria.
Alternativa: lo screening solo nei pazienti con altri fattori di rischio cardiovascolare e renale sembra giustificato, a condizione che loro siano disposti a controllare più strettamente i fattori di rischio quando sono a conoscenza della microalbuminuria.
3. Neuropatia diabetica (28)
- La polineuropatia diabetica è eterogenea e presenta manifestazioni cliniche diverse (può anche essere focale e asimmetrica). La polineuropatia simmetrica è la più comune. Tuttavia, devono essere ricercati anche i sintomi della polineuropatia autonomica (tachicardia a riposo, intolleranza alla performance, ipotensione ortostatica, stipsi, gastroparesi, disfunzione erettile)
- Il più delle volte, la polineuropatia diabetica è una diagnosi di esclusione e non richiede esami particolari.
Nota: in caso di polineuropatia grave, è necessario considerare ed escludere altre cause (ad es. carenza di vitamina B12, HIV, ipotiroidismo, storia di alcolismo, insufficienza renale).
Esame neurologico
- Sensibilità superficiale: monofilamento plantare lato metatarsale 1–2, plantare distale su alluce (mai su aree cornificate). Il monofilamento è affidabile anche in età avanzata
- Sensibilità profonda: riflessi (RA, PSR), senso di posizione, vibrazione (norma
≥ 5/7, al raggio I mediale dell’articolazione di base ≤ 4/8).
Nota: Il riflesso achilleo e il senso di vibrazione possono essere assenti a livello bimalleolare anche in persone sane di età superiore ai 70 anni.
–> Consultare un neurologo se- Predominano i deficiti motori piuttosto che quelli sensoriali
- I sintomi si sviluppano o progrediscono rapidamente (nonostante un buono stato metabolico)
- La sintomatologia inizia da estremità superiori.
Nota: non tutte le polineuropatie associate al diabete mellito sono polineuropatie diabetiche.
4. Controllo dei piedi
- Controllo 1 volta all’anno, più spesso nei diabetici mal controllati. Informarsi sui piedi ad ogni visita
- Fare attenzione a
- La pelle: colore, turgore, ragadi, vesciche, calli, emorragie subcutanee
- Le scarpe: abbastanza larghe, piatte?
- Lo stato del polso
- Ipercheratosi e formazione di calli
- Lesioni del piede, ipo- o anidrosi
- Segni di infezione batterica/o micosi
- Deformità dei piedi (ad es. artropatia di Charcot, dita di martello, dita ad artiglio)
- Ulcera del piede con indicazione della localizzazione, dell’estensione e dell‘infezione concomitante.
- Misure
- Lavare i piedi ogni giorno, fare la doccia, il pediluvio è sconsigliato a causa dell’ammorbidimento, temperatura dell’acqua non superiore a 30 gradi, asciugare sempre bene i piedi (non usare il phon) e applicare una crema neutra (olio di mandorle, schiuma Allpresan, Dexeryl, ecc.)
- Scuotere le scarpe prima di metterle (per rimuovere i corpi estranei)
- In caso di desquamazione (l’ipercheratosi è uno dei principali segni della neuropatia diabetica: il paziente non suda più), ad es. Excipial® 10 % urea (no pomate contenenti salicilato o Allpresan® schiuma per piedi)
- Accorciare le unghie solo con lime di cartone o con Maniquick (smerigliatrice adatta)
- Trattare le micosi in modo coerente. Eccezione micosi ungueale –> vedi mediX GL Onicomicosi
- I pazienti dovrebbero rivolgersi a un podologo medico ogni 3 mesi perché il 70 % di pazienti non è in grado di valutare i propri piedi a causa del deterioramento dell’acuità visiva.
Nota: la podologia è coperta dall’assicurazione di base se c’è un’ulcera o una polineuropatia. Altrimenti solo dall’assicurazione complementare.
- Trattare precocemente malposizioni, calli, punti di pressione con plantari.
-
Trattamento della polineuropatia distale
- Controllare bene il diabete, indicazione alla terapia insulinica
- Dolori superficiali: terapia locale con capsaicina 0,075 % 4 volte al giorno. Pomata alla capsaicina (0,025–0,1 %), sollievo dal dolore nella polineuropatia provato (28), ma rischio di effetti collaterali irreversibili (ad es. disturbi sensoriali) (3, 26).
mediX non raccomanda questa sostanza ai diabetici! - Dolore profondo: farmaci antiepilettici (38, 39) come il gabapentin (ad es. Neurontin®, generici) 900–3’400 mg (titolare) (27), pregabalin (Lyrica®), duloxetin (Cymbalta®). Tutti hanno la stessa efficacia e devono essere scelti in base al profilo degli effetti collaterali de alla co-morbilità.
Farmaci di riserva: antidepressivi triciclici come imipramina (Tofranil®) 25–75 mg, amitriptilina (Saroten®) 25–75 mg, clomipramina (Anafranil®) 25–150 mg - Eventualmente provare il trattamento con Dafalgan® alla sera.
- Fare attenzione a
5. Controllo cardiologico
- Solo in presenza di un‘anamnesi di sintomi cardiaci, non di routine.
3.5. Diabete e guida
- I diabetici devono soddisfare le seguenti condizioni per ottenere l’autorizzazione iniziale o il mantenimento dell’autorizzazione alla guida di veicoli a motore
- Nessun effetto tardivo del diabete rilevante per la guida (acuità visiva insufficiente, disturbi del campo visivo, neuropatia o malattie cardiovascolari che influiscono sul funzionamento del veicolo)
- Nessuna iperglicemia significativa, in particolare nessun innalzamento del livello di glucosio nel sangue associato a sintomi generali con effetti sulla capacità di guida
- Inoltre, è necessario determinare il rischio individuale di ipoglicemia in base al tipo di terapia scelta e alla percezione dell‘ipoglicemia (vedi tabella 3).
Tabella 3: rischio di ipoglicemia e misure per i conducenti del 3° gruppo medico (secondo [40])

Informazioni dettagliati sono reperibili nelle linee guida della SSED
SEED: Linee guida sull’idoneità alla guida e sulla capacità di guida nel diabete mellito (2017); scheda informativa per i conducenti con diabete.
3.6. Diabete gestazionale
Diagnosi
- Screening in tutte le donne in gravidanza tra la 24a e la 28a settimana di gestazione, in caso di rischio aumentato (storia familiare di diabete, stato dopo diabete gestazionale, origine etnica, IMC > 30 kg/m2) dalla 12° settimana di gestazione
- Screening della glicemia a digiuno (8 ore a digiuno): < 4,4 mmol/l (plasma) il diabete gestazionale è escluso
- Glicemia a digiuno ≥ 5,1 mmol/l –> il diabete gestazionale è confermato (senza TOTG!)
- Glicemia a digiuno 4,4–5,0 mmol/l –> esguire TOTG 75 g –> se la glicemia 1 ora
≥ 10 mmol/l e/o 2 ore ≥ 8,5 mmol/l –> il diabete gestazionale è confermato (1) - Esecuzione del TOTG 75 g: 8 ore a digiuno, la donna incinta non deve essere fisicamente attiva e non deve mangiare nulla durante il test
- La determinazione dell‘HbA1c non è rilevante nella gravidanza, poiché i picchi di glicemia postprandiali sono principalmente responsabili dello sviluppo della macrosomia.
Terapia
- Per il 70–80 % delle donne incinte, la dieta è sufficiente; se no: in caso di glicemia a digiuno elevata: insulatard (possibile anche Levemir®/Lantus®, ma più costoso), in caso di glicemia postprandiale elevata: Novorapid®. Nessun antidiabetico orale!
Follow up
- 6–8 settimane dopo la nascita o dopo lo svezzamento: glucosio plasmatico a digiuno e/o TOTG 75 g e/o HbA1c.
Prognosi
- Il diabete gestazionale di solito scompare dopo la fine della gravidanza (a seconda dei valori ICM e della glicemia). Tuttavia, le donne hanno un rischio del 25–60 % di sviluppare il diabete di tipo 2 in seguito. Si consiglia di recuperare il peso precedente alla gravidanza e di fare molto esercizio fisico.
4. Bibliografia
- Kerner W, Brückel J: Definition, Klassifikation und Diagnostik des Diabetes mellitus. Diabetologie 2011; 6: 107 S110.
- Bopp M, et al.: Routine Data Sources Challenge International Diabetes Federation Extrapolations of National Diabetes Prevalence in Switzerland. Diabetes Care. 2011; 34(11): 2387–2389.
- Empfehlungen der Schweizerischen Gesellschaft für Endokrinologie und Diabetologie (SGED/SSED) für die Behandlung von Diabetes mellitus Typ 2 (2023).
- Tabák AG, et al.: Prediabetes: a high-risk state for diabetes development. Lancet 2012; 379: 2279–2290.
- Schweizerische Gesellschaft für Endokrinologie und Diabetologie: Messung des HbA1c zur Diagnose des Diabetes mellitus – Stellungnahme der SGED/SSED (2011).
- Borm K, et al.: Erste Behandlungsschritte beim neuentdeckten Diabetes mellitus Typ 2 – praktische Tipps. Schweiz Med Forum 2012;12(48):929–935.
- Management of Hyperglycemia inType2 Diabetes: A Patient-Centered Approach Position Statement of the American Diabetes Association (ADA) and the European Association the Study of Diabetes (EASD). Diabetes Care 2012; 35: 1364-79.
- Philippe J, et al.: Massnahmen zur Blutzuckerkontrolle bei Patienten mit Typ-2-Diabetes-mellitus Consensus statement der Schweizerischen Gesellschaft für Endokrinologie und der Diabetologie (SGED). Schweiz Med Forum 2009; 9(3):50-55.
- UKPDS-Folgestudie – Was folgt für die Diabetestherapie? arznei-telegramm 2009; 40:74-5.
- Duckworth W, et al.: Glucose control and vascular complications in veterans with type 2 diabetes. N Engl J Med. 2009 Jan 8;360(2):129-39.
- Vitamin-B12-Mangel unter Einnahme von Metformin. Arznei-telegramm 2012:43:29-30.
- Mamtani R, et al.: Association Between Longer Therapy With Thiazolidinediones and Risk of Bladder Cancer: A Cohort Study. NCI: Journal of the National Cancer Institute, Volume 104, Issue 18, 19 September 2012, Pages 1411–1421.
- Gangji AS, et al.: A systematic review and meta-analysis of hypoglycemia and cardiovascular events: a comparison of glyburide with other secretagogues and with insulin. Diabetes Care 30 (2007) 389-394.
- Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen: Glinide zur Behandlung des Diabetes mellitus Typ 2. 4/2009.
- Neues orales Antidiabetikum: DPP-IV-Hemmer Sitagliptin (Januvia®). Arznei-telegramm 2007; 38: 56-7.
- Orales Antidiabetikum Vildagliptin. Arznei-telegramm 2008; 39: 66-7.
- Antidiabetikum Liraglutid (Victoza®) – Plädoyer für die Marktrücknahme. Arznei-telegramm 2012; 43: 64.
- IQWiG-Abschlussbericht: Langwirksame Insulinanaloga bei Diabetes mellitus Typ 2 (2009).
- Holman RR, Thorne KI, Farmer AJ, et al.: Addition of biphasic, prandial, or basal insulin to oral therapy in type 2 diabetes. N Engl J Med 2007 (25. Oktober); 357: 1716-30.
- IQWiG-Bericht: Urin- und Blutzuckerselbstmessung bei Diabetes mellitus Typ 2 (2005).
- Stöckli R, Zimmerli L: Hypertonie und Diabetes. Schweiz Med Forum 2009;9(36):626-629.
- AHA: Aspirin and heart disease (aufgerufen 7/2020).
- Low-Dose Aspirin for Primary Prevention of Atherosclerotic Events in Patients With Type 2 Diabetes. A Randomized Controlled Trial. JAMA 2008;300(18):2134-2141. doi:10.1001/jama.2008.623.
- Diuretika und Diabetes mellitus. Arznei-telegramm 2008; 39: 3-4.
- Nationale Versorgungsleitlinie. Nierenerkrankungen bei Diabetes im Erwachsenenalter. 11/2011. http://www.diabetes.versorgungsleitlinien.de/.
- Mason L, et al.: Systematic review of topical capsaicin for the treatment of chronic pain. BMJ 2004;328(7446):991.
- Masche U: Antiepileptika bei neuropathischen Schmerzen. Pharma-kritik. 15/2005.
- Nationale Versorgungsleitlinie Neuropathie bei Diabetes im Erwachsenenalter. 4/2012. http://www.diabetes.versorgungsleitlinien.de/.
- McBrian K, et al.: Intensive and Standard Blood Pressure Targets in Patients With Type 2 Diabetes Mellitus Systematic Review and Meta-analysis. Arch Intern Med. 2012;172(17):1296-1303.
- Lipska KJ, et al.: Use of Metformin in the Setting of Mild-to-Moderate Renal Insufficiency. Diabetes Care 2011; 34(6): 1431–1437. http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3114336/.
- deJager J, et al.: Long term treatment with metformin in patients with type 2 diabetes and risk of vitamin B-12 deficiency: randomised placebo controlled trial. BMJ 2010 (20. Mai); 340: c2181.
- Clar C, et al.: Systematic review of SGLT2 receptor inhibitors in dual or triple therapy in type 2 diabetes. BMJ Open. 2012;2(5).
- IQWiG-Bericht: Dapagliflozin – Nutzenbewertung gemäß § 35a SGB V (2013).
- Scirica BM, et al.: Saxagliptin and Cardiovascular Outcomes in Patients with Type 2 Diabetes Mellitus. N Engl J Med 2013; 369:1317-1326.
- ESC/EAS-Dyslipidämie-Guidelines. Swiss Med Forum. 2020;20(0910):140-148. https://doi.org/10.4414/smf.2020.08464.
- Petrie MC, et al.: Effect of Dapagliflozin on Worsening Heart Failure and Cardiovas-cular Death in Patients With Heart Failure With and Without Diabetes.JAMA.2020;323(14):1353–68.
- Solomon SD, et al.: DELIVER Trial Committees and Investigators.Dapagliflozin in Heart Failure with Mildly Reduced or Preserved Ejection Fraction. N Engl J Med. 2022;387(12):1089–98.
- Nationale Versorgungsleitlinie: Neuropathie bei Diabetes im Erwachsenenalter. 08/2011 (zuletzt geändert 01/2015).
- NICE-Guideline (CG173): Neuropathic pain in adults: pharmacological management in non-specialist settings (7/2019).
- Arbeitsgruppe SGED, SDG, SGRM: Richtlinien bezüglich Fahreignung und Fahrfähigkeit bei Diabetes mellitus (2017).
- Green JB, et al.: Effect of Sitagliptin on Cardiovascular Outcomes in Type 2 Diabetes. N Engl J Med 2015; 373:232-242.
- Jornayvaz FR: Erstbehandlung bei Verdacht auf Diabetes mellitus. Swiss Medical Forum 2015;15(47):1097-1103.
- Marso SP, et al.: Liraglutide and Cardiovascular Outcomes in Type 2 Diabetes. N Engl J Med 2016; 375:311-322.
- American Diabetes Association: Pharmalogic effects of glycemic treatment. Diabetes Care, Volume 43, Supplement 1, January 2020.
- Neal B, et al.: CANVAS Program Collaborative Group:Canagliflozin and Cardiovascular and Renal Events in Type 2 Diabetes. N Engl J Med. 2017;377(7):644.
- US Preventive Services Task Force: Aspirin to prevent cardiovascular disease: preventive medication, 04/2022.
- He L, Wang J, Ping F, et al.: Association of Glucagon-Like Peptide-1 Receptor Agonist Use With Risk of Gallbladder and Biliary Diseases: A Systematic Review and Meta-analysis of Randomized Clinical Trials. JAMA Intern Med.2022;182(5):513–519.
- McMurray JJV, et al.: DAPA-CKD Trial Committees and Investigators. Effect of Dapagliflozin on Clinical Outcomes in Patients With Chronic Kidney Disease, With and Without Cardiovascular Disease. Circulation. 2021 Feb 2;143(5):438-448.
- Echouffo-Tcheugui JB, Perreault L, Ji L, Dagogo-Jack S: Diagnosis and Management of Prediabetes: A Review. 2023;329(14):1206–1216. doi:10.1001/jama.2023.4063.
- Albert SG, Wood EM, Ahir V: Glucagon-like peptide 1-receptor agonists and A1c: Good for the heart but less so for the eyes? Diabetes Metab Syndr. 2023 Jan;17(1):102696. doi: 10.1016/j.dsx.2022.102696. Epub 2022 Dec 28. PMID: 36596264.
5. Appendice
Tabella 4: gli antidiabetici in sintesi
|
Farmaci antidiabetici |
Preparati (esempi) |
Vantaggi |
Svantaggi |
|
Farmaci di prima linea ben validati |
|||
|
Metformina |
(Metfin®, Glucophage®) |
Neutri dal punto di vista del peso |
Effetti collaterali gastrointestinali |
|
Insulina |
|
Nessun limite di dose, azione rapida, migliora il profilo lipidico |
Monitoraggio, ipoglicemia, aumento di peso, analoghi dell’insulina costosi |
|
Sulfoniluree |
Gliclazide (Diamicron® e |
Azione rapida, usare soloil gliclazide! |
Aumento di peso, ipoglicemia, (soprattutto glibenclamide)
|
|
Farmaci ben validati (principalmente) per la terapia combinata |
|||
|
Agonista GLP-1 |
Liraglutide (Victoza®), |
Perdita di peso, cardio (e nefro-)protettivo |
Iniezione, effetti collaterali gastrointestinali, costoso |
|
Inibitore SGTL-2 |
Dapagliflozin (Forxiga®), Canagliflozin (Invokana®, Vokanamet®), |
Perdita di peso, lieve riduzione della pressione sanguina, cardio- e nefroprotettivo |
Rischio di infezioni genitali significativamente aumentato (circa del 10 %), soprattutto nelle donne
|
|
Gliptini (inibitori della DPP-IV) (anche in combinazione con la metformina) |
Saxagliptin (Onglyza®, |
Neutri dal punto di vista del peso |
Costosi, neutri dal punto di vista cardiovascolare; necessario l’adattamento renale (eccetto linagliptin), controllare i valori epatici con vitagliptin
|
|
Antidiabetici non raccomandati |
|||
|
Inibitori dell’alfa-glucosidasi |
Acarbose (Glucobay®) |
Neutro dal punto di vista del peso |
Effetti collaterali gastrointestinali, dosaggio 3 volte al giorno, costoso |
|
Pioglitazone |
Actos® |
Migliora il profilo lipidico |
Ritenzione di liquidi, aumento di peso, rischio di fratture, tumore alla vesica (?), costoso |
|
Glinidi |
Repaglinide (NovoNorm® e generici), |
Nell’insufficienza renale a causa dell’emivita breve |
Dosaggio multiplo giornaliero, aumento di peso, ipoglicemia, costoso |
Tabella 5: Compendio degli antidiabetici e limitazioni
|
Antidiabetici |
Preparati (esempi) |
Limitazioni |
|
Farmaci di prima linea ben validati |
||
|
Metformina |
(Metfin®, Glucophage®) |
Nessuna |
|
Sulfoniluree |
Gliclazide (Diamicron® e generici) |
Nessuna |
|
Insuline |
|
Nessuna |
|
Farmaci ben validati (principalmente) per la terapia combinata |
||
|
Agonisti del GLP-1
|
Liraglutide (Victoza®)
|
· In combinazione con metformina, una SU o una combinazione di metformina e una SU o di metformina e pioglitazone se questi AO non consentono di ottenere un adeguato controllo glicemico · In combinazione con l’insulina di base solo nei pazienti con un controllo glicemico inadeguato dopo una precedente terapia con metformina e Victoza® · Almeno IMC 28. Ulteriori farmaci per la perdita di peso non sono rimborsati dall’assicurazione malattie |
|
Dulaglutide (Trulicity®) |
· In combinazione con metformina o una combinazione di metformina e una SU o metformina e pioglitazone se i trattamenti con metformina e le rispettive combinazioni doppie non sono sufficientemente efficaci · In combinazione con l’insulina prandiale (a breve durata d‘azione) +/- metformina, solo nei pazienti con un controllo inadeguato della glicemia dopo una terapie precedente con metformina e Trulicity · Almeno IMC 28. Ulteriori farmaci per la perdita di peso non sono rimborsati dall’assicurazione malattie |
|
|
Semaglutide (Ozempic®, Rybelsus®) |
· Per il trattamento di pazienti con diabete mellito di tipo 2; solo nelle seguenti terapie combinate, se non si ottiene un controllo glicemico adeguato con questi antidiabetici · Come combinazione di due farmaci con metformina o una sulfonilurea · In tripla combinazione con una combinazione di metformina e una sulfonilurea · In combinazione con insulina di base con o senza metformina · Almeno IMC 28. Ulteriori farmaci per la perdita di peso non sono rimborsati dall’assicurazione malattie |
|
|
Gliptini (inibitori della DPP-IV)
|
Saxagliptine (Onglyza®, |
· Solo in combinazione con metformina, una SU, pioglitazone o con insulina se non si ottiene un controllo glicemico adeguato con gli AO attuali o se uno degli AO non è tollerato · Come triplice terapia solo in combinazione con metformina e una SU, se non si ottiene un controllo glicemico adeguato con metformina e SU (come combinazione di due farmaci) · Terapie combinate con altri AO OAD –> approvazione da parte dell’assicurazione malattie dopo aver consultato il medico di fiducia |
|
Sitagliptine (Januvia®, |
· Per i pazienti che non possono essere controllati adeguatamente con gli attuali AO e/o insulina o che non li tolleranno · Terapie combinate con altri AO eccetto SU e/o insulina –> approvazione da parte dell’assicurazione malattie dopo aver consultato il medico di fiducia |
|
|
Vildagliptine (Galvus®, |
· Per i pazienti che sono controllati inadeguatemente con gli AO attuali o che non li tolleranno · Come doppia combinazione con metformina o SU o glitazone se metformina o SU o glitazone da soli non forniscono un controllo glicemico sufficiente · Come tripla combinazone con metformina e SU se la doppia combinazione con queste sostanze non fornisce un adeguato controllo glicemico · In combinazione con insulina (+/- metformina), se la dieta, l‘esercizio fisico e una dose stabile di insulina non forniscono un adeguato controllo glicemico · Terapie combinate con altri AO –> approvazione del medico di fiducia dell’assicurazione malattie |
|
|
Linagliptine (Trajenta®, |
· Per i pazienti con un controllo inadeguato o intolleranti agli attuali AO · In combinazione solo con metformina, una SU, glitazone o una combinazione di metformina e SU se non si ottiene un controllo glicemico adeguato con questi AO · Terapie combinate con altri AO –> approvazione dell’ assicurazione malattie, previa consultazione del medico di fiducia |
|
|
Alogliptine (Vipidia®, |
· Solo in combinazione con metformina, una SU o con insulina se non si ottiene un controllo glicemico adeguato con i farmaci attuali · Terapie combinate con altri antidiabetici –> approvazione dell’assicurazione malattie, previa consultazione del medico di fiducia |
|
|
Inibitore del SGLT-2 |
Empagliflozin (Jardiance®, |
· Come monoterapia nei pazienti che non possono essere trattati con metformina · In combinazione con metformina da sola o in combinazione con una SU o insulina, da sola o in combinazione con metformina e/o sulfonilurea se non si ottiene un controllo sufficiente della glicemia con questi trattamenti · Terapie combinate con altri AO –> approvazione da parte dell’assicurazione malattie dopo aver consultato il medico di fiducia |
|
Dapagliflozin (Forxiga®) |
· Come monoterapia se la dieta e l’attività fisica aumentata non consentono di ottenere un controllo glicemico adeguato · In combinazione con AO (metformina, inibitori della DPP4, SU) e/o insulina (+/- metformina), se questi farmaci non forniscono un controllo glicemico sufficiente · Terapie combinate con altri antidiabetici –> approvazione da parte dell’assicurazione malattie dopo aver consultato il medico di fiducia |
|
|
Canagliflozin (Invokana®, |
· Come monoterapia nei pazienti che non possono essere trattati con metformina · In combinazione con metformina, con SU (+/- metformina) o insulina (+/- metformina) se questi trattamenti non consentono di ottenere un controllo glicemico sufficiente · Combinazione con altri antidiabetici –> approvazione da parte dell’assicurazione malattie dopo aver consultato il medico di fiducia |
|
|
Antidiabetici non raccomandati |
||
|
Inibitori dell’alfa-glucosidasi |
Acarbose (Glucobay®) |
Nessuna |
|
Pioglitazone |
Actos® |
· Usare quando i livelli HbA1c non possono essere raggiunti con altri antidiabetici orali standard |
|
Glinidi |
Repaglinide (NovoNorm® e generici), |
Nessuna
|
6. Informazioni legali
|
Questa guideline è stata completamente rivista e aggiornata nel marzo 2024. Editrice Redazione Autori |
Questa guideline è stata creata senza influenze esterne con la collaborazione di tutte le reti mediX regionali e delle reti associate. Non vi sono dipendenze finanziarie o di contenuto dall'industria o da altre organizzazioni o gruppi di interesse. Se non diversamente specificato, ciò vale espressamente anche per gli autori della linea guida. Le guidelines mediX contengono raccomandazioni terapeutiche per specifici disturbi o situazioni di trattamento. Tuttavia, ogni paziente deve essere trattato in base alla sua situazione individuale. Sebbene le guidelines mediX siano sviluppate e controllate con grande cura, l’associazione mediX schweiz non può assumersi alcuna responsabilità per la loro correttezza, in particolare per quanto riguarda le informazioni sul dosaggio. Tutte le Linee guida mediX su Internet al indirizzo www.medix.ch L’associazione mediX schweiz è un’associazione di reti di medici e di medici in Svizzera. Si prega di inviare un feedback a: uwe.beise_at_medix.ch |